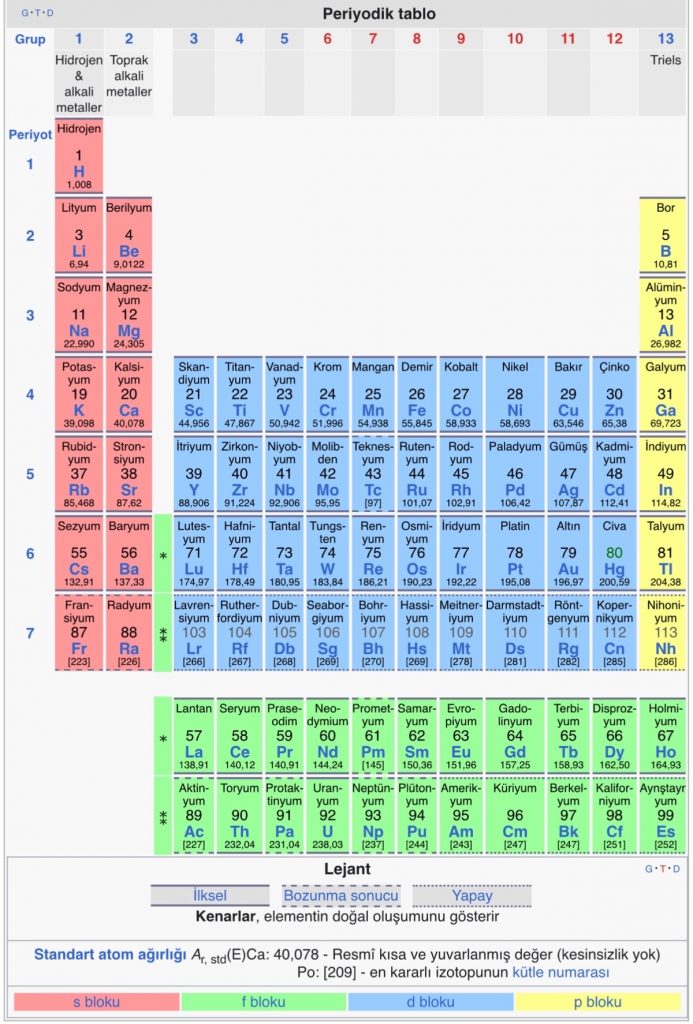
Periyodik tablo, kimyasal elementlerin sınıflandırılması için geliştirilmiş tablodur. Dilimizde periyodik tablo, periyodik cetvel, periyodik çizelge, elementler tablosu gibi birçok şekilde isimlendirilmiştir.
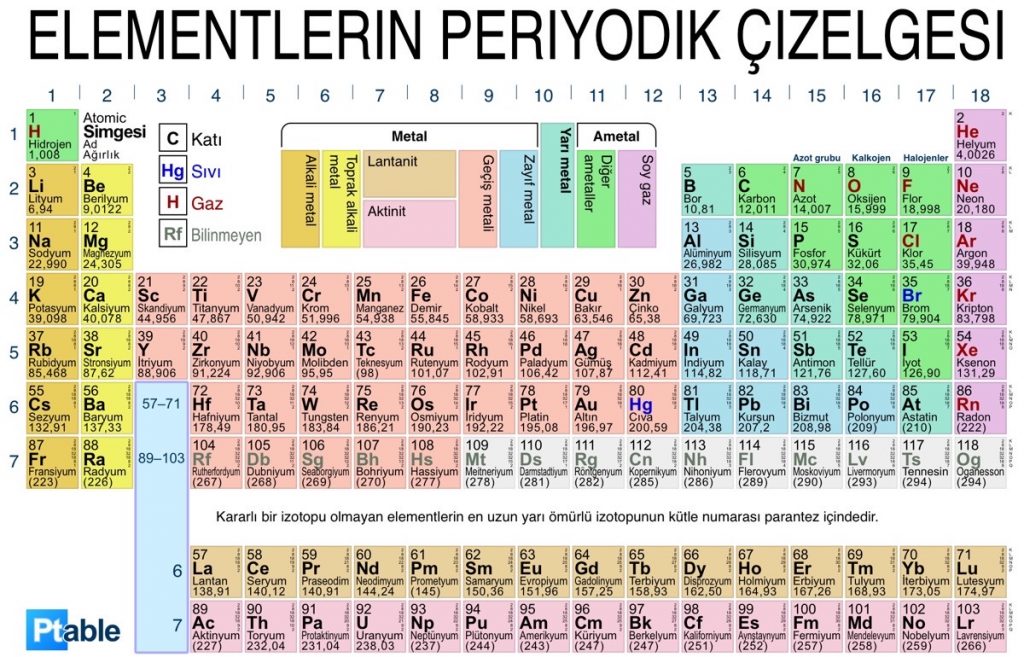
Bu tablo bilinen bütün elementlerin artan atom numaralarına (buna proton sayısı da denir) göre bir sıralanışıdır. Periyodik cetvelden önce de bu yönde çalışmalar yapılmış olmakla birlikte, mucidi genelde Rus kimyager Dmitri Mendeleyev kabul edilir.
Periyodik tabloyu kim bulmuştur ya da bulunmasına yardım edenler kimlerdir?
Periyodik tablonun bulunmasında en önemli katkıyı Rus kimyager Dmitri Mendeleyev yapmıştır. Mendeleyev, 1869 yılında bilinen 63 elementin atom kütlelerini inceleyerek, bu elementlerin atom kütlelerine göre düzenli bir şekilde sıralandığını fark etmiştir. Bu sırayla, benzer özelliklere sahip elementlerin bir arada geldiğini gözlemlemiştir. Örneğin, aynı grupta yer alan elementler benzer kimyasal özelliklere sahiptir.
Mendeleyev’in bu çalışması, periyodik tablonun temellerini atmıştır. Daha sonra, diğer bilim insanları da periyodik tabloyu geliştirmeye devam etmiştir. 1913 yılında, İngiliz kimyager Henry Moseley, elementlerin atom numaralarının, atomlarının çekirdeğindeki proton sayısını gösterdiğini keşfetmiştir. Bu keşif, periyodik tablonun daha da geliştirilmesine yardımcı olmuştur.
Günümüzde, periyodik tabloda 118 element yer almaktadır. Bu elementlerin 92’si doğal olarak bulunurken, 26’sı yapay olarak üretilmiştir.
Periyodik tabloda yer alan maddelerin türleri nedir?
Periyodik tabloda yer alan maddeler, atomlarının dış kabuklarında bulunan elektron sayısına göre farklı türlere ayrılır. Bu türler şunlardır:
- Alkali metaller: Dış kabuklarında 1 elektron bulunan elementlerdir. Bu elementler, yumuşak, parlak ve kolayca oksitlenebilirler.
- Alkali toprak metalleri: Dış kabuklarında 2 elektron bulunan elementlerdir. Bu elementler, alkali metallere göre daha serttir ve daha az oksitlenebilirler.
- Geçiş metalleri: Dış kabuklarında 1, 2 veya 3 elektron bulunan elementlerdir. Bu elementler, genellikle parlak ve serttirler.
- Toprak alkali metalleri: Dış kabuklarında 2 elektron bulunan elementlerdir. Bu elementler, alkali toprak metallerine göre daha yumuşaktır ve daha kolay oksitlenebilirler.
- Halogenler: Dış kabuklarında 7 elektron bulunan elementlerdir. Bu elementler, genellikle parlak ve renklidirler.
- Ametaller: Dış kabuklarında 5, 6 veya 8 elektron bulunan elementlerdir. Bu elementler, genellikle kırılgan ve oksijenle kolayca reaksiyona girerler.
- Soygazlar: Dış kabuklarında 8 elektron bulunan elementlerdir. Bu elementler, genellikle inerttirler ve kimyasal reaksiyonlara girmezler.
Kaç grup var?
Periyodik tabloda 18 grup bulunmaktadır. Her gruptaki elementler, dış kabuklarında aynı sayıda elektrona sahiptir. Bu nedenle, gruptaki elementler benzer kimyasal özelliklere sahiptir.
Bilinen kaç madde var?
Günümüzde, periyodik tabloda 118 element yer almaktadır. Bu elementlerin 92’si doğal olarak bulunurken, 26’sı yapay olarak üretilmiştir.
Bilinmeyen ama olması gereken kaç madde vardır?
Periyodik tablonun sonu, henüz tam olarak bilinmemektedir. Teorik olarak, periyodik tabloda 120’ye kadar element bulunması beklenmektedir. Ancak, bu elementlerden henüz hiçbiri keşfedilmemiştir.
Periyodik tablo, kimya biliminin temellerini oluşturan önemli bir araçtır. Bu tablo, elementlerin özelliklerini ve kimyasal reaksiyonlarını anlamak için kullanılır.
© 2024 – 2023, Bedri Yılmaz.
BedriYilmaz.com by Bedri Yılmaz is licensed under Attribution-NonCommercial-NoDerivatives 4.0 International